research 研究紹介
Outline 研究概要
リンパ節転移の診断と治療:ナノテクノロジーを用いたがん治療の新たなアプローチ!
がん患者の死因の90%は転移に起因します. そして多くのがん患者においてリンパ節への転移が確認されます. リンパ節転移は, がんが今後どのように進行するのかを示唆する重要な予後因子となりますが,そのメカニズムはいまだ明らかにされていません.

私たちの現在の研究テーマは, 以下の3点です.
- 臨床医学に基づくナノテクノロジーを用いたリンパ節介在血行性転移理論の実験的検証
- リンパネットワークを介した新しいドラッグデリバリーシステムの創製(リンパ行性薬剤送達法: LDDS)
- リンパ節郭清後にともなう遠隔臓器における腫瘍細胞の活性化に関する研究
私たちの研究室では, 既定の概念に固執せず, 私たち自身が, 私たちの手を動かし, 私たち自身が考えるプロセスを通してこれらの命題を解決していきます.
3つのオリジナリティ
Non-clinical trial
1|非臨床試験
20年の歳月をかけて,
リンパ節腫脹マウスを樹立.
リンパネットワークの解明に挑む.
リンパ節転移の研究は, 人間と同じ生命原理で生きる動物による実験でしかその実像に迫ることはできません. マウスを使用した実験,すなわち非臨床試験で得られた成果は, ヒトでおこなう臨床試験へ進める重要な第一ステップとなります.
わたしたちの研究室では, ヒトのリンパ節の大きさと同等の大きさ(直径10mm)を有する, 特殊な「リンパ節腫脹マウス」を独自に樹立し, このマウスを使用した,世界でも希なリンパ節転移研究に特化した実験環境を完備してきました. 臨床医との連携を密にして, 臨床試験につなげる非臨床試験を実施しています.
Drug delivery system
2|独自のDDS
(ドラッグデリバリーシステム)
独自のドラッグデリバリー
システムを開発.
抗がん剤1滴ほどの量で
転移リンパ節への薬剤効果を高める
新たな創薬を目指す.
転移リンパ節の治療では,抗がん剤を使用した全身化学療法が用いられます. しかし,一般的に抗がん剤の多くは副作用をともなうことが多く,奏効率も高くはありません.わたしたちの研究室では, リンパ節に直接抗がん剤を注入することで,このリンパ節だけでなく,このリンパ節のリンパネットワーク下流に位置するリンパ節まで抗がん剤を送達させてがんの治療や予防的治療を目指す, リンパ行性薬剤送達法(lymphatic drug delivery system: LDDS)を開発してきました.LDDSを用いると,全身化学療法で使用される抗がん剤の量に比べてはるかに少ない量に抑えることが可能であると考えております.
近く臨床試験を実施し,近い将来,医薬品の実用化を目指します.
Imaging equipment
Theme
研究テーマ
1.臨床医学に基づくナノテクノロジーを用いた
リンパ節介在血行性転移理論の実験的検証
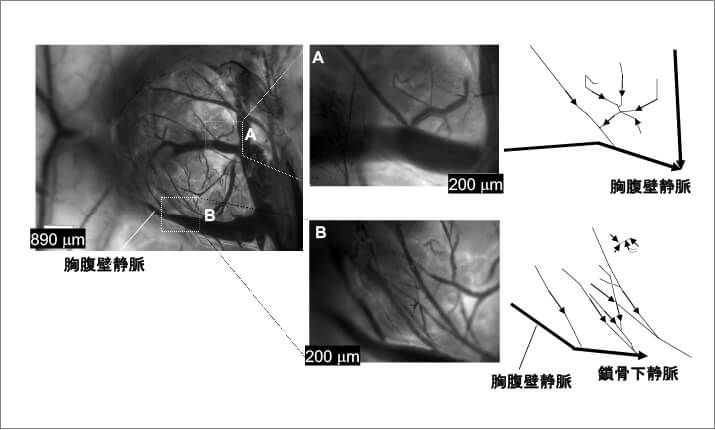
マウスの固有腋窩リンパ節の表面には胸腹壁静脈が走行し, この静脈にはリンパ節内部からの静脈が吻合している(左図). マウスの尾静脈に蛍光粒子を投与すると, 蛍光粒子は固有腋窩リンパ節内の静脈から胸腹壁静脈に流れ込み, 最終的に鎖骨下静脈に流れ出る.
J Cancer Metastasis Treat 2018;4:56.
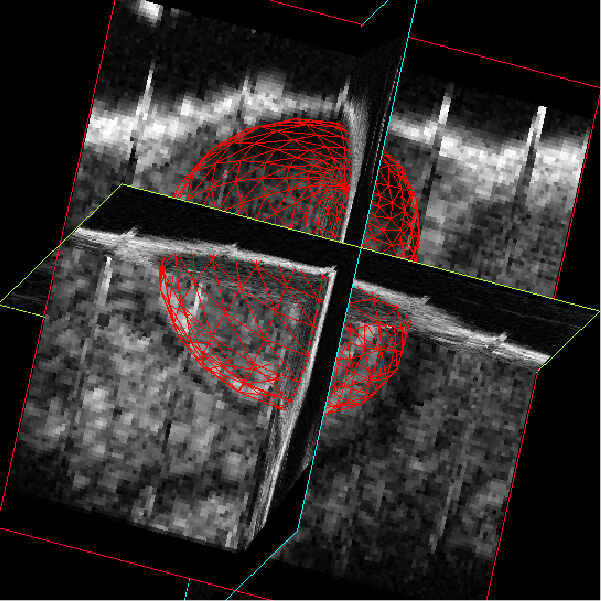
実験データの信憑性を高めるには, 多次元的な解析が必要です. 私たちの研究室では, 分子生物学的手法で形質転換した腫瘍細胞を使用し, その挙動やがんの微小環境を最新の分子イメージング手法(生物発光イメージング法, 高解像度超音波イメージング法, マイクロX線CTイメージング法, 分子病理像)から解析しています.一つの研究室において,これだけの研究規模の装置を自由に使用して成果を挙げることができる研究室は,世界でも稀です.
2.リンパネットワークを介した新しいドラッグデリバリー
システムの創製(リンパ行性薬剤送達法: LDDS)
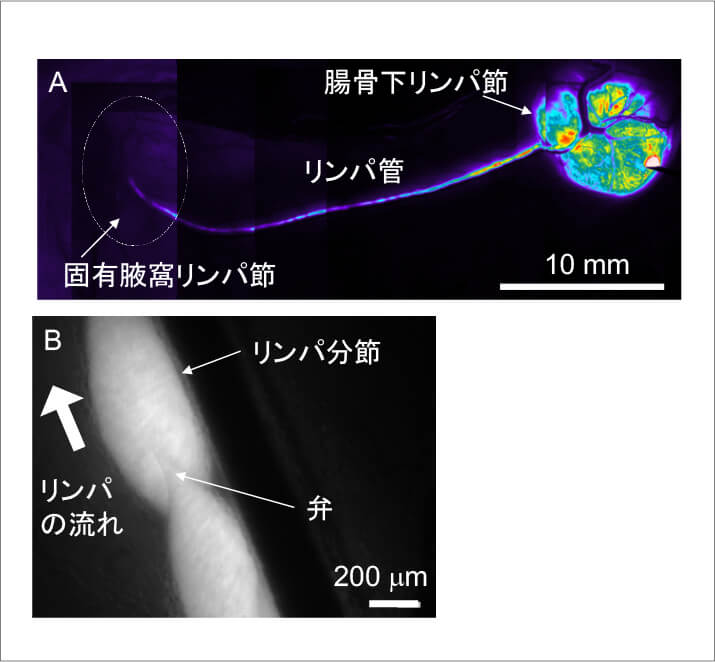
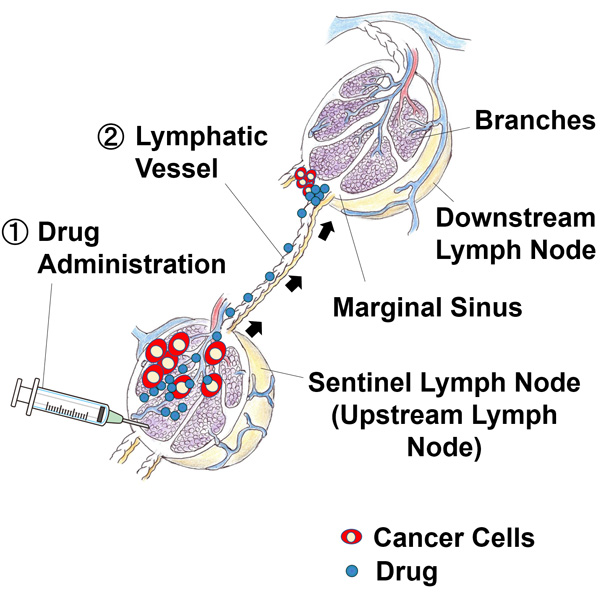
A.腸骨下リンパ節から固有腋窩リンパ節に向かう蛍光色素の流れ.B.リンパ分節と弁.
リンパ管は,リンパ分節と呼ばれる数十個の管が連続して構成されたものである. 各分節には弁があり, リンパの流れの逆流を防ぐ働きがあるため,リンパは一方向に流れる.蛍光色素を腸骨下リンパ節(上流リンパ節)に投与すると,リンパ管を介して固有腋窩リンパ節(下流リンパ節)に流すことができる.したがって,センチネルリンパ節に抗がん剤を注射すると,センチネルリンパ節とその下流リンパ節に転移している腫瘍細胞の治療が期待できる.
Biomed Opt Express. 2015; 6(1):124-34.
リンパ管内の流れ
『リンパ行性薬剤送達法』は, センチネルリンパ節に直接抗がん剤等を注入することで, センチネルリンパ節だけでなく, このリンパ節のリンパネットワーク下流に位置するリンパ節も治療対象にすることができる,本研究室の独創的手法です.
抗がん剤1滴ほどの量で, 転移初期段階にあるひとつのリンパ節を治療することができると見込まれ, この投与量は静脈注射による全身化学療法の投与量に比べ著しく少ない量です。この治療法は, これまで高齢や他の疾患でリンパ節郭清術の適応が困難であった患者や,手術では切除が困難なリンパ節郭清域外のリンパ節も治療できることになり, 抗がん剤の副作用やリンパ節転移に悩む多くのがん患者を救済できる画期的な治療法になるものと期待されます。
2018年11月, PMDAからの承認を得て第Ⅰ相臨床試験の準備段階にあり,本手法の標準治療*を目指しております.
*科学的根拠に基づいて,現在利用できる最良の治療であることが証明されている治療のこと.
3.リンパ節郭清後にともなう遠隔臓器における
腫瘍細胞の活性化に関する研究
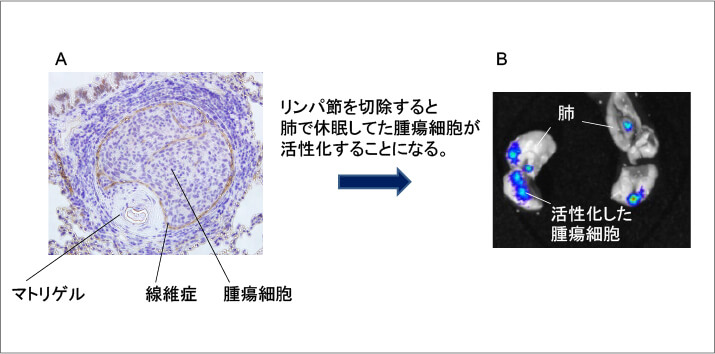
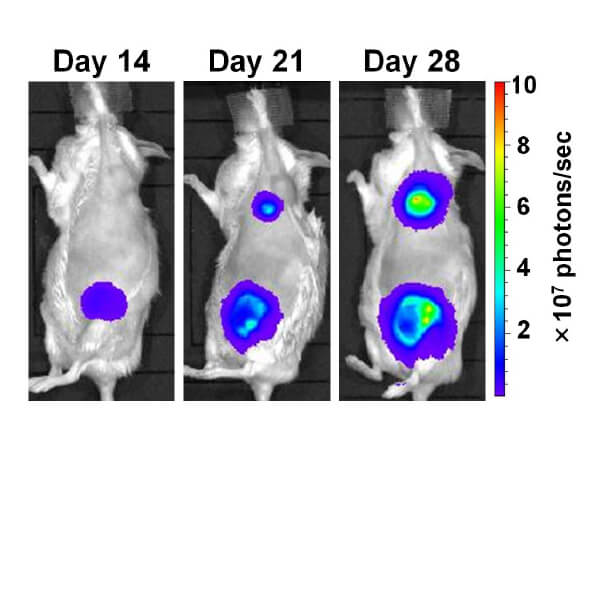
肺に転移したがん細胞は内皮細胞に覆われ休眠状態にある. リンパ節を郭清すると, がん細胞は刺激を受けて増殖を始める.
Biochem Biophys Res Commun. 2015;460:543-8.
Sci Rep. 2019;9(1):16029
臨床において, 腫瘍性リンパ節を切除することで, 局所および遠隔臓器でがん細胞が活性化する例が報告されています. しかしながら, この二つの関連性を実験的に明らかにした研究はこれまで報告されておりません.
わたしたちの研究室では, 本研究室で開発した肺転移活性化マウスモデルを使用して, リンパ節郭清と肺転移腫瘍の活性化との関連性を最新技術で明らかにします.